3분기 매출‧영업익, 직전분기 비 -9.4%‧-58.5% ↓원료약 계약 상황, 계절적 요인 등으로 기저효과 발생 내달 '렉라자' 임상 3상 공개, 내년 1차 치료제로 허가변경 도전국내 피크 매출 1000억원 전망···'학술마케팅' 전력
유한양행은 폐암 신약 '렉라자'(성분명 레이저티닙)의 1차 치료제 사용을 위한 글로벌 임상 3상 시험이 마무리단계에 있는 만큼 단기적으로 수익성 개선이 예상된다는 설명이다.
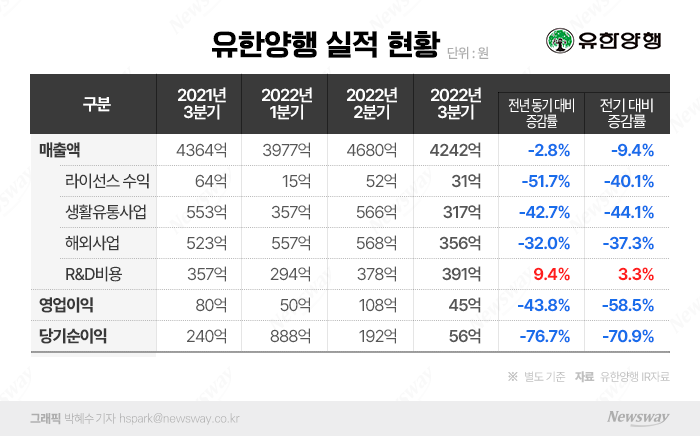
4일 유한양행과 전자공시시스템 등에 따르면, 유한양행의 3분기 별도기준 영업이익은 44억8200만원으로 잠정 집계돼 전년 동기 보다 -43.8%, 직전 분기보다 -58.5% 감소했다. 이에 따라 당기순이익도 55억8600만원으로 전년 동기 대비 76.7%, 직전 분기 대비 70.9% 급감했다. 매출액은 4241억5600만원으로 잠정 집계됐는데, 이는 전년 동기 대비 -2.8%, 직전 분기 대비 -9.4% 감소한 수치다.
3분기 실적 하락은 생활유통사업, 해외사업, 라이선스 수익 감소와 R&D 비용 증가의 영향이 컸는데, 시기적‧계절적 요인이 반영됐기 때문이라고 회사 측은 설명했다.
락스, 살충제 등의 제품을 판매하는 생활유통사업 매출은 올 3분기 316억6500만원으로, 전년 동기 대비 42.7%, 직전 분기 대비 44.1% 감소했다. 원료의약품 사업을 주로 영위하는 해외사업 매출은 355억8900만원으로, 전년 동기 대비 32%, 직전 분기 대비 37.3% 감소했다. 라이선스 수익은 31억원으로 지난해 대비 51.7%. 직전 분기 대비 40.1% 감소했다.
회사 측은 "생활유통사업은 여름 시즌이 끝나고 코로나 엔데믹 상황이 맞물리며 시장 수요가 감소했다. 해외사업의 경우 원료의약품 수출이 대부분을 차지하는데, 계약물량이라 파트너사의 사정이나 협의 내용에 따라 (실적이) 달라질 수 있다"라고 말했다.
이어 "물론 거래처가 있긴 하지만 의약품처럼 루틴하게 매주 판매되는 게 아니라서 휴지기가 있을 수밖에 없다. 특히 올 상반기 실적이 전년 대비 50~60% 크게 성장하는 등 초반에 집중된 경향으로 기저효과가 반영됐다고 볼 수 있다"면서 "매출이 축소되다 보니 이익 감소가 이뤄졌는데, 주력 의약품 사업은 9.7% 성장을 견조하게 이어가고 있다"라고 부연했다.
라이선스 수익과 관련해서는 "단계별 성과금(마일스톤)은 계약 후 임상 진입 등 다음 스텝으로 넘어가는 이벤트가 있어야 발생하고, 초기 임상보다는 후기 임상으로 진입했을 때 금액이 커진다. 올해는 인식되는 게 없는 상황"이라고 했다.
R&D 비용 증가도 수익성 악화에 영향을 끼쳤다. 회사의 3분기 R&D 비용은 390억원으로, 전년 동기보다 9.4%, 직전 분기보다 3.3% 증가했다.
하지만 폐암 신약 '렉라자'를 단독 투여하는 글로벌 임상 3상 시험이 막바지에 다다른 만큼 향후 전반적인 실적 개선 가능성은 높다. 회사 측은 "R&D 비용에서 큰 부분을 차지하고 있던 게 렉라자 단독 임상인데, 현재 거의 마무리 단계에 있어 단기적으로는 계속 투여되던 비용 부담이 줄어들 것"이라며 "1차 치료제 사용을 위한 글로벌 임상 3상 시험 데이터는 다음 달 3일 싱가포르에서 열리는 '유럽종양학회(ESMO) 아시아'에서 공개할 예정이다"라고 말했다.
렉라자는 상피세포 성장인자 수용체(EGFR)에 변이가 있는 비소세포폐암 환자에 쓰는 항암제다. 지난해 1월 식품의약품안전처로부터 국내에서 31번째로 개발된 신약으로 허가받았다.
현재는 기존 1·2세대 표적항암제 등 1차 치료 이후 사용할 수 있는 2차 치료제로 쓰이는데, 1차 치료제로 사용할 수 있는지를 파악하기 위해 아스트라제네카의 '이레사정'(성분명 게피티니브)과 비교해 효과를 검증하는 글로벌 임상 3상 시험이 진행돼 왔다. 회사가 지난 달 공개한 무진행 생존 기간 비교 결과에서는 렉라자가 질병 진행 혹은 사망 위험을 55% 감소시키는 것으로 나타났다.
업계에서는 렉라자가 1차 치료제 시장에 안착할 경우 연간 매출이 1000억원을 상회할 것으로 보고 있다.
EGFR 돌연변이 비소세포폐암 1차 치료제 시장 규모는 약 3000억원 정도다. 이 질환은 아시아인에게서 주로 발견되는데, 현재 1차 치료제로 주로 쓰이고 있는 아스트라제네카의 '타그리소'는 한국인을 포함한 아시아 환자들에게 아쉬운 임상 데이터를 보이고 있어 건강보험 급여 문턱을 넘지 못하고 있다.
회사 측은 "이번 임상3상 결과를 토대로 내년 초 식약처에 1차 치료제로 허가 변경을 신청할 계획"이라며 "경쟁약물이 글로벌 제약사의 제품이고, 허가 시기도 빨라 임상 데이터가 더 많이 쌓였겠지만 항암제라는 약물 특성과 질환의 위중성이 있기 때문에 의사 및 환자들에게 렉라자의 강점을 꾸준히 알릴 필요가 있다. 학술 마케팅 등을 통해 신뢰를 높이고 시장을 확대해 나갈 것"이라고 밝혔다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
<저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지>






















댓글